
La micropropagation
-A quoi sert la micropropagation?
Elle sert à régénérer des plantes entières à partir de n'importe qu'elle partie de cette dernière.
-De quelle partie se sert-on?
De toute, une feuille, un bourgeon, une racine, une cellule.
-Cela parait trop beau, où est l'arnaque?
Il n'y en a pas, cette technique est utilisée dans les laboratoires de recherche, et depuis peu dans les grandes exploitation, permettant de multiplier à l'infini une plante avec des caractères spéciaux.
Maintenant, la technique à proprement parler et la vérification scientifique, par la suite je rajouterai comment le faire simplement à moindre coût et sans aucune connaissance.
Introduction
Outre l'utilisation récréative du cannabis, d'autres comme la production de fibre, de graines à alimentation humaine ou encore de production de molécules pharmaceutiques existent.
Ce type d'application à fort coût économique a très vite intéressé les chercheurs. Cependant le cannabis jouissant dune réputation défavorable très peu de publication sont accessibles.
Néanmoins, pour moi la science devant être partagée et surtout pas gardée comme un secret, je vais vous révéler la technique la plus performante à l'heure actuelle pour obtenir une quantité impressionnante de boutures dans un laps de temps fort court.
Matériel et méthodes
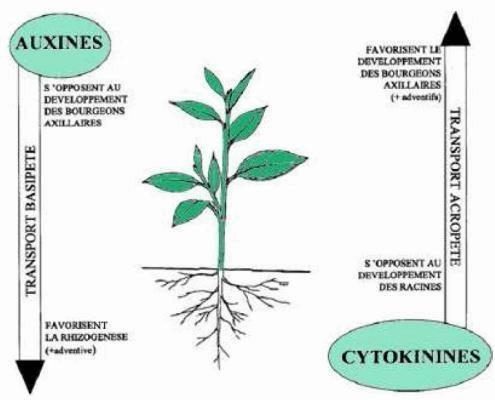
-Germination de graines à l'obscurité dans un milieu de 90% d'humidité pendant 24h.
-Stérilisation à l'hypochlorite de calcium 5% pendant 6-8-15 minutes.
-Puis remise en germination dans une solution aqueuse à 3% de glucose et 1% de saccharose.
-Suivit de la mise en croissance hors sol de plantes.
-Arrivé à 3 semaines de croissances les plantes sont sacrifiés.
-On part alors de pétiole, d'entre nœud, de bourgeons axillaires et du bourgeon apical.
-Mise en culture dans boite d'Agar-agar pré-stérilisé à l'autoclave, 120°C pendant 45 min.
-Puis les cultures sont placées à l'obscurité pendant 3 semaines, en présence d'une balance hormonale favorisant la différenciation des cellules en type racine. Cette enceinte est maintenu à 22°c.
-Puis passage en mode éclairage à 22°c, sous photo période de 16/8.
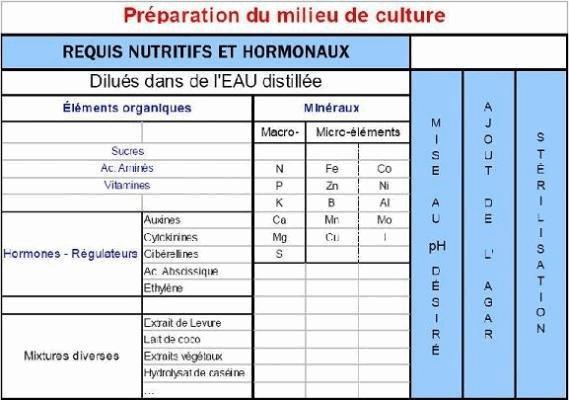

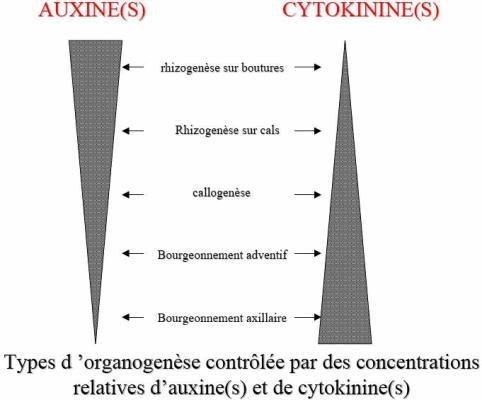
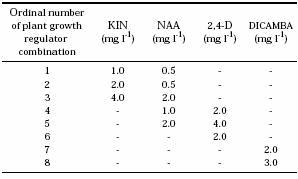
-Pour la formation des racines, les plantules régénérées à 2 cm de haut ont été cultivés sur MS basal moyen complété avec 1,0 mg l-1 IAA (Auxine) et 1,0 mgl-1 NAA. Les plantes enracinées ont été transférées vers le sol et cultivées dans une serre.
Statistiques
Expériences impliquant quatre explants, cinq cultivars et une moyenne de huit combinaisons ont été réalisées dans une étude complète (RCB) de conception en trois répétitions.
L'effet des régulateurs de croissance des végétaux sur l'induction pour les différents explants (jeunes feuilles, pétioles,entrenœuds, bourgeons axillaires) a été exprimé en pourcentages. Pour savoir si les résultats étaient significatifs ,nous avons utilisé Two-way ANOVA, et normalisé la distribution.

Résultats
La stérilisation des explants a été meilleure en remuant la solution d'hypochlorite de calcium 5% pendant 15 min.
Toutes les préparations ont pu être régénérées en entier, donnant naissance à des lignées génétiquement identiques mais phénotypiquement différentes. En effet partant de plantes dioïques strictes femelles nous sommes arrivés à des phénotypes hermaphrodites ou plutôt d'inter-sexes.
Ce phénomène a cependant été contrôlé conduisant à une restauration du phénotype femelle, partant de là une autre étude sera faite pour expliquer cette dédifférenciation ou comment partir de plantes hermaphrodites et induire une différentiation perpétuelle en un seul sexe de manière irréversible.
Discussion
Il faut préciser que les meilleures régénération ont été obtenues à partir de pétioles et de feuilles, de plus le bourgeon apical à été régénéré aussi bien en présence qu'en absence d'hormone, sa régénération sur milieu gélosé n'est donc pas obligatoire.
Expérimentation facilitée
I-Introduction
Cette technique va permettre de régénérer une plante quelle que soit la partie prélevée, mais pour des soucis de technicité et de compétences, nous allons étudier le cas de la régénération par des cellules de parenchymes chlorophyllien de feuille (Pouvoir réducteur sous forme de NADPH(2)+ pour les curieux).
Outre l'aspect pratique de pouvoir préparer des milliers de boutures identiques au pied mère en partant de n'importe qu'elle partie de la plante, la micropropagation offre bien d'autres ouvertures plus que passionnantes et gorgées de surprises.
En conclusion je vous expliquerai comment croiser vos meilleures plantes mères et les régénérer pour donner naissance à des plantes au potentiel végétatif et floristique pratiquement infini.
Je tiens également à dire que ces protocoles sont ma propriété intellectuelle et qu'aucune utilisation à but lucratif ou associatif ne peut avoir lieu sans ma permission sous risque de poursuites mais l'utilisation personnelle est autorisée. Merci
II-Matériel et méthodes
Liste du matériels à se procurer :
- Un scalpel végétal
- De l'alcool à 90%
- Une gazinière ou mieux un bec Bunsen
- Votre plante à micropropager
- Récipient pour micropropager ( boite de pétri, tube à essai, pot yaourt....)
- Une pipette précision 0.1ml
- Auxine 1mg/L
- Cytokinine 1mg/L
- Du milieu minérale MS ou Murashige ou Skoog
(Tout cela est facilement trouvable sur internet, en cas de problème je rajouterais les adresse où en trouver)
Avertissement :
- Les hormones ne supportent que très mal la température (elles sont thermolabiles), il est conseillé de les conserver au réfrigérateur à +/- 4°c. Et de ne les sortir que pour les expériences.
- Le milieu MS ou autres sont vendus en poudre, il faudra les compléter à l'eau et les faire chauffer au bain marie bouillant pour qu'ils se dissolvent, mais attention à bien les garder à cette température car une fois refroidis il durcissent et sont inutilisables.
- Toute les manipulations doivent se dérouler avec le plus de stérilité possible. Désinfecter le plan de travail, vos mains, tout le matériel, puis allumer votre bec Bensen (flamme blanche) et délimiter un rayon de 20 à 30 cm autour qui constituera votre cône de stérilité ou vous manipulerez.
Tout se passe dans le cône de stérilité
Préparation des milieux :
- Désinfectez vos boites à l'alcool, puis au bain marie à 80°c pendant 5 min, puis laissez sécher.
- Chauffez votre solution (milieu ms + eau jusqu'au col de la bouteille) au bain marie bouillant, pensez à laisser le bouchon ouvert. Une fois totalement dissout au bout de 30 à 60 minutes, laissez refroidir légèrement pendant 5 min puis coulez dans vos boites sur environ 1 cm de profondeur. (conservation 3 semaines maximums)
- Minimum 2 boites par expérience, sur la première mettre 1mg/L d'auxine ( 0.5 ml)+ 1mg/L de cytokinine (0.5ml) nous permettra d'obtenir de Cals. Noté MSAC
Et sur la deuxième, mettre 0.1mg/l d'auxine (0.5ml) + 1mg/L de cytokinine (0.5ml), ne pas oublier de bien homogénéiser sur tout le substrat. Nous permettra de régénérer, noté MSEL
Prélèvement des fragments à micropropager :
- Prendre une feuille d'aluminium, la désinfecter au bain marie 80°c pendant 5 min, puis à l'alcool et la garder dans le champ stérile. Cette feuille permettra de stériliser le matériel végétal.
- Prendre une feuille de votre plante et la placer entre deux morceaux d'aluminium, laisser en contact 3 min, puis découper un carré de 1cm de coté, en prélevant une partie de la nervure centrale.
- Mettre les fragments sur les milieux, sceller les boites avec du scotch ou de la parafilm et placer les boîtes 3 semaines à 1 mois à température 18-20°c et faiblement éclairé.
III-Résultats
Les milieux MSEL vont développer des bourgeons, de là, rajouter de l'auxine et elles feront des racines, il ne reste plus qu'à les replanter en terre.
Les milieux MSAC vont former des amas de cellules indifférenciées et immortelles, en abaissant la température à 10°c vous pouvez les garder en quiscence pendant plusieurs années, et en prélever pour effectuer de la régénération sur milieu MSEL.
Il est donc facile de conserver des dizaines de génétiques dans sont frigo et de les régénérer au moment voulu. Cette technique permet la pérénité des variétés et un approvisionnement constant en bouture sélectionnées sur un phénotype intéressant afin de produire des boutures à l'infini.
IV-Discussions et évolutions
Le principe de la régénération peut également être utilisé pour réaliser des croisements, ceux-ci étant rendus impossibles soit par le nombre de générations demandées (10 ou 20 000), par le nombre de chromosomes inadéquates, par des notions de dominances récessivités, etc...
La solution se trouve dans la génération de protoplastes (cellules végétales ayant perdu leurs paroi). Puis dans la fusion de deux protoplastes venant de plantes différentes. On obtient donc une cellule possédant les deux génomes et exprimant toutes les particularités des deux plantes. Sans compter qu'elles sont donc au minimum tétraploïdes (voir beaucoup plus) et que du coup les stocks d'hormones de croissance et de floraison sont doublés.
Il suffit donc de régénérer ces protoplastes fusionnés en micropropagation, et l'on obtient des plantes monstrueusement résistantes et productives, sans compter qu'elles peuvent être bouturées ou micropropagées à l'infini.
Voici la technique mise en vidéo :
v/c Dad-
-
 1
1
-
 7
7


