
N°1 :
"la nutrition azotée"
INTRODUCTION
Les végétaux terrestres tirent généralement leur azote du sol, sous forme de nitrates ou de sels d'ammonium, produits de décompositions organiques dues aux micro-organismes présents dans ces sols.
A noter les plantes actinorhiziennes qui réalisent avec des organismes symbiotiques une synthèse d'ammoniaque à partir du diazote de l'air (Rhizobium), propriétés également dévolue à certains microorganismes libres.
L'azote est un nutriment primaire indispensable aux végétaux, il est souvent donné à titre de valeur indicative dans les engrais(N-P-K).
Il s'agit d'un macro-élément libre dans le continuum sol-plante, et même au sein de la plante. Il va déterminer plusieurs paramètres clef du cycle de vie de la plante, ce que nous allons voir.
1/ L'azote dans le continuum sol-plante-atmosphère
1.A/L'azote du sol
Sous nos climats dans une bonne terre végétale, la teneur en azote est de l'ordre d' 1g/kg de terre, soit environ 5T d'azote / hectare.
Sur cette masse ,1 à 2% sont sous forme minérale (en moyenne), le reste sous forme organique, humus principalement.
La matière organique des sols provient principalement des déchets végétaux, les déchets animaux ne représentant qu'une faible part de celle-ci.
Ces déchets, une fois décomposés et réorganisés par la microflore, sont minéralisés, donc transformés en substances minérales, beaucoup plus facilement assimilables par la plante.
Principalement du NH4+ (et NH4OH) , secondairement oxydé en NO3-,CO2 (et HCO3-),H2PO4-, avec libération des cations (CA2+,MG2+,K+ etc.) et anions CL- qui étaient plus ou moins liés à elles.
_Œuvre de bactéries cellulolytiques (cytophaga) et protéolytiques (proteus), la dégradation porte essentiellement sur la cellulose et les protéines, et est rapide (ordre de grandeur quelques semaines à quelques mois). Elle aboutit à la dégradation d'environ 70% de l'humus du sol
Les résidus sont de diverses formes dont la composition dépend de la nature des débris et donc du type de végétation.
On y trouve notamment les acides humiques et fulviques ainsi que l'humine.
1.B/L'azote minéral
La première étape de l'élaboration de l'azote minéral est l'ammonisation, réalisée par des bactéries.
Par exemple:
_pour les amines:
Molécule carbonée-NH2+H2O -> R-COOH+NH3
Il s'agit d'une hydrolyse d'une molécule contenant une fonction amine produisant un acide carboxylique et une molécule d'ammoniac
_pour les aminoacides:
NH2-Molécule carbonée-COOH+H2O -> R-CH2OH+CO2+NH3
Il s'agit d'une hydrolyse d'un acide aminé en dioxyde de carbone, en ammoniac et un alcool primaire.
L'étape suivante, la nitrification conduit à la formation de nitrates. Deux types de bactéries entrent en compte dans cette étape:
_ les bactéries nitreuses, réalisant la nitrosation :
(NH4+)+(2/3 O2) -> (NO2-)+(H2O)+(2H+)
_les bactéries nitriques, qui oxydent :
(NO2-)+(1/2 O2) -> NO3-
Ces réactions sont des oxydoréductions, les bactéries de la nitrification sont dites chimiotrophes car elles tirent leur énergie de l'oxydation d'un substrat extérieur.
2. L'utilisation de l'azote
Nous tâcherons de montrer comment la plante utilise l'azote durant son développement, par quelles réactions et à quelles fins.
2.A/ L'utilisation de l'azote organique
Le cannabis est capable d'assimiler l'azote sous forme organique lorsqu'il s'agit de petites molécules (aminoacides, glutamine, urée, acide urique) bien que le rendement soit faible comparé à une alimentation nitrique ou ammoniacale.
2.B/L'utilisation de l'azote minéral
ammoniacal- nitrique
La plupart des plantes cultivées ont un rendement meilleur avec les nitrates. La réduction de ceux-ci leur coute de l'énergie, mais branchée sur le catabolisme glucidique, cette dégradation favorise la production d'acide cétonique.
Généralement les plantes jeunes préfèrent le NH4+ (ce n'est cependant pas une généralité)
Il est à noter l'importance du pH:
Un abaissement de pH facilite l'absorption et l'assimilation des nitrates, alors que son élévation favorise celle des ions ammonium.
La teneur en sucre également, en particulier des racines, qui dépend étroitement de l'activité photosynthétique du végétal, conditionne la nutrition azotée.
En effet à partir des glucides solides se fabriquent les acides cétoniques qui permettront l'incorporation de l'azote en aminoacides.
2.C/Les engrais azotés
Il est possible de les classifier en 3 ordres :
Les engrais ammoniacaux :
Sulfate, chlorure ou phosphate d'ammonium.
Ce sont des engrais acidifiants, utilisés en terre et administrés dès la préparation du substrat (engrais de fond).
Ils présentent le double avantage d'être mis à la disposition de la plante au fur et à mesure de ses besoins sans atteindre ses doses toxiques et d'empêcher leur entrainement par les arrosages successifs.
En effet les ions NH4+ s'adsorbent sur les colloïdes du sol, et sont échangés par des ions H+ issus de la plante.
Leur absorption ne fait donc pas fluctuer le pH du substrat.
Les engrais nitriques :
Nitrates de sodium, calcium ou potassium.
Ils conviennent pour des interventions rapides. Il est conseillé de les appliquer au moment même où ils sont requis.
Les complexes ammoniacaux-nitriques :
Nitrates d'ammonium...
Ils permettent de cumuler les avantages de l'un et l'autre, fournissant un apport immédiat à la plante et également un apport progressif lié aux évolutions de consommation de la plante.
3/L'assimilation de l'azote
La réduction des nitrates
La réduction commence en général dans la racine, bien que chez beaucoup d'espèces la réduction s'effectue également dans la feuille mise à la lumière (alors qu'il n'y a pas de photorécepteurs pour les racines, en revanche le pouvoir réducteur des feuilles est du NADPH2 et celui des racines du NADH2, ce qui fait des feuilles de meilleurs usines de réduction).
La réduction dans son ensemble représente un gain de 8 électrons :
(NO3-)+(8H+)+(8e-) -> NH3+(2*H2O)+OH- (9-;1-) = 8-
Cette réduction s'effectue en deux étapes, qui s'enchainent très vite : la réduction des nitrates en nitrites, et la réduction de ceux ci en NH3 :
(NO3-)+(2H+)+(2e-) -> (NO2-)+(H2O)
(NO2-)+(6H+)+(6e-) -> (NH3)+(H2O)+(OH-)
Fait établi en 1924 par S.ECKERSON (USA).
D'autres étapes intermédiaires sont probables mais non vérifiables, comme la transition par l'hydroxylamine NH2OH. En effet les nitrites sont toxiques à haute dose, ce qui corrobore le fait que la réduction s'opère sans discontinuer et à des doses non létales pour l'organisme végétal.
4/Utilisation de l'azote
4.A/Durant la croissance
Le rapport de l'azote est très dépendant de son rapport avec le carbone :
D'une façon générale une alimentation riche en azote favorise le développement végétatif au détriment de l'appareil reproducteur.
Au contraire une alimentation carbonée abondante favorise la floraison. C’est ainsi qu'une photosynthèse active est indispensable.
D'où l'importance du rapport C/N qui est (en masse) en moyenne de l'ordre de 20. Autour de cette moyenne, sans pouvoir fixer de mesures très précises bien sur, le développement dépend en grande mesure du rapport C/N :
C/N très élevé: développement végétatif faible (carence azotée).
C/N élevé : abondante production fruitière.
C/N faible : développement végétatif vigoureux.
C/N très faible : faible développement végétatif (carence carbonée).
Il a été constaté, dans les plantes dont la floraison dépend de la photopériode (donc cannabis compris), que le taux de saccharose dans la sève phloèmienne augmentait fortement au passage à la floraison, il apparaitrait donc que cet afflux de saccharose, sans en être le facteur déterminant, soit un important facteur de l'induction florale (donc du stretch) et non un signal de floraison.
4.B/Mouvements et stockage durant la période de stretch
- Cas d'un sol riche en azote
Durant le stretch, la plante va augmenter le nombre de transporteurs d'azote (HATS) au niveau des racines et va également augmenter leurs enzymes de métabolisation; la nitrate réductase et la nitrite réductase. Tout cet azote prélevé au niveau du sol va alors remonter dans la plante via la sève brute. Cette augmentation brutale de la concentration d'azote va induire la formation d'une zone tampon pour le stockage transitoire de cet azote.
Ceci se traduit par une augmentation du volume totale de tige, et la levée de dormance des bourgeons secondaires. Dans ce cas le stockage s'effectue donc dans les tiges et les bourgeons situés au niveau des apex secondaires peu développés ainsi que des apex tertiaires...
- Cas d'un sol pauvre en azote
La plante n'agit donc pas sur ses racines, pour éviter de dépenser de l'énergie inutilement étant donné la faible présence de l'azote dans le sol.
Dans ce cas l'azote va donc être reconcentrée dans la tige à l'aide d'une sénescence précoce des vieilles feuilles, toujours du bas vers le haut, ainsi qu'à partir de la dégradation des acides aminés présents dans la tige.
N'ayant pas assez d'azote pour effectuer une levée de dormance complète, celui-ci sera préférentiellement stocké dans la tige et également au niveau des bourgeons secondaires situés au plus près de la canopée, par un mécanisme lux-dépendant.
En conclusion, on peut donc dire que la majorité de l'azote se retrouve au niveau des tiges tampon élaborées pendant le stretch et un peu également au niveau des bourgeons.
La concentration de l'azote de la tige et le nombre de bourgeons réveillés varient en fonction de la concentration en azote.
5/Utilisation des stocks après induction florale
Après l'induction florale, la zone tampon n'a plus d'utilité en tant que telle.
La zone avec la force de puits la plus grande va donc pouvoir diriger le flux d'azote grâce aux pressions osmotique et hydrique.
Ces pressions se font en réalité par deux mécanismes :
- Le premier est une relation d'osmose, où la cellule source va stocker les éléments dans sa vacuole afin de former un gradient décroissant de soluté de la source vers elle. Ce qui par la notion d'équilibre va attirer l'azote stocké dans les tiges, mais pas celui stocké dans les bourgeons.
- Le second mécanisme est la perte de pression osmotique par synthèse d'osmoticum, comme les sucres et autres afin là aussi de générer un gradient décroissant.
Pour les bourgeons, la force de puits provoquée par l'induction florale bloque totalement l'azote présent et attire également celui de la tige.
Cet azote se trouve essentiellement sous forme d’acides aminés. Ceux -ci vont être stockés à excès dans les bractées puis, si la concentration en azote est adéquate, la plante va former des feuilles ressources. C'est à dire de petite feuilles avec une activité photosynthétique globale inférieure à 0 (non auto-suffisante). Ces feuilles ont la tache de retenir l'azote et surtout d'entretenir la force de puits de part leur activité photosynthétique.
En conclusion, l'azote se retrouve mobilisé en grande partie par les futures têtes et par les feuilles présentes dans ces têtes.
5.A/Dans le cas de sinsemilia
S’il n'y a pas formation de graine, la totalité de l'azote part vers les bractées et les feuilles ressources sans pouvoir en sortir.
Préférentiellement stocké sous forme d'acides aminés et quelques dérivés ammoniacaux.
La force de puits y est telle que le reste de la plante peut mourir, ces parties resterons vertes. La seule technique pour le faire sortir est d'augmenter la température et de descendre l'hygrométrie tout en rinçant sévèrement la plante.
5.B/Dans le cas de semilia
Dans ce cas la grande majorité de l'azote est transféré à la graine via le micropyle, il est stocké sous forme d'acides aminés, de protéines HSP et de protéines de réserve.
Dans ce cas il est préférable d'éviter l'étape de rinçage et de continuer à fournir de faibles quantités d'azote durant toute la floraison.
5.C/Utilisation de l'azote et déclenchement de la sénescence
Lors de la phase de stretch, la plante va stimuler son absorption d'azote via les racines afin de former des tissus de réserves pour alimenter les futures graines. Durant cette phase la plante est en capacité maximale d'absorption des nutriments.
Cependant cette augmentation de métabolisme, conduisant à une sur-activation de l'anabolisme de l'azote et des autres constituants, va gravement épuiser les racines de la plante; qui va consécutivement à cela subir une détérioration des transporteurs racinaires complète pour les transporteurs de l'azote et de 20 à 50% pour les autres transporteurs. Seul les aquaporines (transporteurs passif de l'eau) restent intactes.
Suite à ce phénomène la plante va stocker l'azote absorbé dans des nouveaux tissus, une fois les stocks épuisés, la plante va détruire les vieilles feuilles afin d'y récupérer encore plus d'azote aboutissant à la sénescence.
Les mécanismes globaux de la sénescence sont contrôlés génétiquement et peuvent varier d'une espèce à l'autre, au niveau date de déclenchement, durée et intensité du phénomène.
Une sénescence précoce est souvent le résultat d'un manque d'engraissage azoté durant la période de stretch et est très dure à réguler.
6/Relations azote - floraison
L'azote à deux grands rôles au niveau de la floraison :
- Déclenchement de la multiplication florale post-croissance végétative maximum (stretch). En effet le taux d'azote emmagasiné dans les zones tampon va dicter la puissance de l'induction florale, car seul cet azote sera disponible, dû à la perte d'efficacité d'absorption des HATS vis-à-vis de l'azote de la solution du sol.
Paradoxalement le taux accumulé pendant cette période va déterminer la date d'apparition des premiers organes de reproduction; mais également leurs nombres futur (dans le cas ou aucun apport exogène en foliaire n'est ajouté).
Il est donc très important de ne pas négliger l'apport en cet élément durant la croissance mais aussi durant la période de stretch.
- Déclenchement de la sénescence et maturation des composants florifères (Bractées, trichome, pistil ...) La sénescence est l'évènement par lequel l'azote piégé dans les vieilles feuilles adultes va être remobilisé par une force de puits extrêmement forte au niveau des zones sous méristématiques (Bourgeons et têtes). Ce phénomène ne se produit que lorsque la plante a totalement perdu sa faculté à prélever l'azote du sol par ses racines.
Ce phénomène est très important car par lui se produit l'abscision foliaire des vieilles feuilles et des structures devenues non essentielles. La plante en profitant pour se débarrasser dans ses parties du maximum d'éléments toxiques jusqu'à présent stockés (seulement ceux ne rentrant pas en compte dans la pression osmotique).
Une fois toutes ces parties tombées, la force de puits devient extrêmement forte et la plante peut de nouveau absorber de manière optimale les autres éléments (et ce malgré sa faiblesse racinaire). Ce phénomène dicté par l'azote va permettre à la plante de recevoir un trop plein d'éléments (surtout P/K/S et Malate citrate) qui vont alors déclencher une forte réponse de maturation globale de la plante.
La maturation va d'abord toucher les zones à la force de puits la plus grande et ainsi de suite (du haut vers le bas, du tronc principal vers les extrémités).
Dernière étape, une fois la force de puits équilibrée, un signal d'oxydation des composés secondaires est envoyé (protection à long terme des organes portant les graines) conduisant à la maturation de ces métabolites secondaires (Comme le THC et ses dérivés).
7/Relations azote - éthylène
Le cannabis n'étant pas une plante climactérique, l'éthylène n'a pas d'action de maturation. Elle est une hormone de stress pouvant provoquer l'abscision foliaire et le blocage en quiescence des méristèmes végétatifs ou floraux.
En ce sens un manque d'azote produit un stress minéral négatif pouvant, si couplé à un stress hydrique, stimuler la production d'éthylène.
De même un surplus d'azote couplé à un sur ou sous arrosage va stimuler la production d'éthylène et provoquer la synthèse d'acide abscissique aboutissant à une chlorose et à une perte de feuilles atteintes.
8/Gestion des ressources
8.A/La régénération
Pour régénérer un pied, l'amendement en azote est un élément primordial de la reprise de croissance, mais dépend de l'état du système racinaire.
Comme dit précédemment le NH3 est principalement dégradé dans la racine et il peut être préférable de s'occuper en priorité de la rhizogènese (AIA,AIB ou stimulateurs racinaires) avant d'ajouter de l'azote, de préférence des complexes ammoniacaux-nitriques, qui auront à la fois un effet immédiat et plus durable.
8.B/Azote, feuillage et photosynthèse
Nous pouvons mettre en corrélation azote, feuillage et photosynthèse...
azote -> feuillage -> photosynthèse
photosynthèse +assimilation d'azote -> feuillage -> photosynthèse
Conclusion : donnez de l'azote en quantité à vos plantes durant la croissance végétative, elles vous le rendront bien...
8.c/L'élimination du N
Afin de limiter le mauvais gout, il peut être intéressant d'éliminer un maximum d'azote de la plante, pas trop tôt pour ne pas perdre en rendement, mais suffisamment pour assurer une meilleure qualité de produit fini.
Conclusion générale et techniques d'améliorations
Après ces explications un peu complexes, voici ce qu'il faut retenir.
Pendant la croissance l'azote est très demandé par la plante mais uniquement par voie racinaire, tout ajout par voie foliaire va diminuer l'absorption racinaire de l'azote et des autres éléments et donc ralentir la croissance en générale.
Pendant la phase de stretch la consommation en azote est très forte car celui-ci est accumulé dans des organes tampons comme les tiges et les pétioles. La demande est telle qu'un engraissage racinaire ne suffit pas à remplir ces organes tampons, un complément foliaire peu alors être ajouté pour permettre à la plante d'exprimer tout son potentiel productif au niveau organe de reproduction. C'est à ce moment que la masse finale des têtes est déterminée par la plante. Plus le potentiel de source des organes de réserves va être faible, plus les gènes architectes responsable du nombre, de la taille, et de la densité des Buds vont être actifs.
Puis une fois en floraison, la plante perd entre 70 et 95 % de ces propriétés d'absorptions racinaires pour l'azote mais également pour les autres éléments nécessitant un transport actif. Pour pallier à un manque d'azote ou tout autre élément outres P, K, un engraissage foliaire sera la meilleure technique. Vous pouvez également, après deux à trois semaines d'induction de floraison, rajouter du nitrate de calcium par voie foliaire afin non seulement d'ajouter de l'azote pour augmenter la masse sèche finale mais également rajouter du calcium qui est le messager secondaire le plus important chez les plantes, et qui dès lors va augmenter la transduction des signaux métaboliques et permettre à la plante de métaboliser au maximum ses ressources.
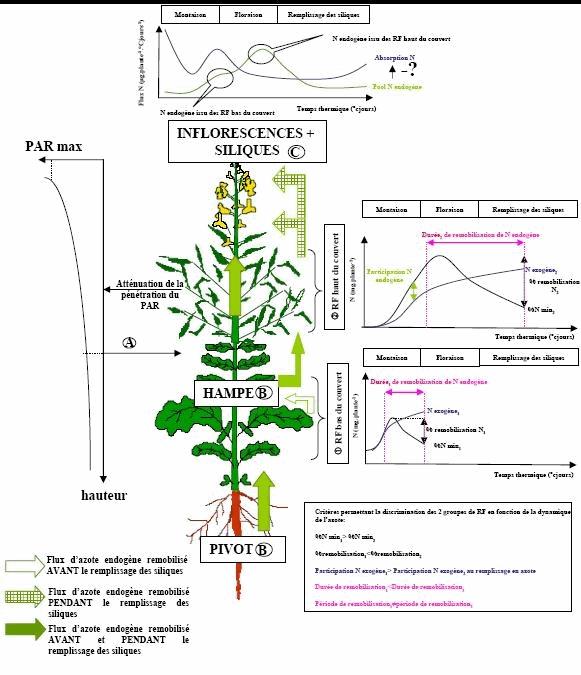
Schéma récapitulatif global :
Sources:
physiologie végétale 2eme cycle, 6e édition de l'abrégé, DUNOD
nutrition- développement; R.Heller,R.Esnault,C.Lance
synthèse et mise en page par ER²
Source Malagoli et al 2004,2006,2006
SMRI pour l'analyse isotopique des mouvement d'azote par le rapport N13/N15 et N/C.
Diepenbrock W. 2000. Yield analysis of winter oilseed rape (Brassica
napus L.): a review. Field Crops Research 67: 35–49.
Dreccer MF, Schapendonk AHM, Slafer GA, Rabbinge R. 2000.
Comparative response of wheat and oilseed rape to nitrogen
supply: absorption and utilisation efficiency of radiation and nitrogen
during the reproductive stage determining yield. Plant and Soil 220:
189–205.
Gabrielle B, Denoroy P, Gosse G, Justes E, AndersonMN.1998.Amodel
of leaf area development and senescence of winter oilseed rape. Field
Crops Research 57: 209–222.
Habekotte´ B. 1997. Identification of strong and weak yield determining
components of winter oilseed rape compared with winter wheat.
European Journal of Agronomy 7: 315–321.
Hocking PJ, Randall PJ, DeMarco D. 1997. The response of dryland
canola to nitrogen fertilizer: partitioning and mobilization of dry matter
and nitrogen, and nitrogen effects on yield components. Field Crops
Research 54: 201–220.
Jensen LS, Christensen L, Mueller T, Nielsen NE. 1997. Turnover of
residual N-15-labelled fertilizer N in soil following harvest of oilseed
rape (Brassica napus L.). Plant and Soil 190: 193–202.
Laine´ P, Ourry A, Macduff JH, Boucaud J, Salette J. 1993. Kinetic
parameters of nitrate uptake by different catch crop species: effects
of low temperatures or previous nitrate starvation. Physiologia
Plantarum 88: 85–92.
Lawlor DW. 2002. Carbon and nitrogen assimilation in relation to yield:
mechanisms are the key to understanding production systems. Journal
of Experimental Botany 53: 773–787.
Leleu O, Vuylstecker C, Teˆtu JF, Degrande D, Champolivier L,
Rambour S. 2000. Effect of two contrasted N fertilisations on
rapeseed growth and nitrate metabolism. Plant Physiology and
Biochemistry 38: 639–645.
Lemaire G, Gastal F. 1997. N uptake and distribution in plant canopy. In:
Lemaire G, ed. Diagnosis of the nitrogen status in crops. Heidelberg:
Springer Verlag, 3–43.
Lemaire G, Onillon B, Gosse G, ChartierM,AllirandJM.1991. Nitrogen
distribution within lucerne canopy during regrowth: relation with
light distribution. Annals of Botany 68: 483–488.
Malagoli P, Laine´ P, Le Deunff E, Rossato L, Ney B, Ourry A. 2004.
Modeling N uptake in Brassica napus L. cv Capitol during a growth
cycle using influx kinetics of root nitrate transport systems and field
experimental data. Plant Physiology 134: 388–400.
Merrien A, Palleau JP, Maisonneuve C. 1988. Besoins en e´le´ments
mine´raux du colza cultive´ en France. In: Physiologie et e´laboration
du rendement du Colza. Paris: Cetiom Editions, 34–46.
Nanda R, Barghava SC, Rawson HM. 1995. Effect of sowing date on
rates of leaf appearance, final leaf numbers and areas in Brassica
campestris, B. juncea, B. napus and B. carinata. Field Crops Research
42: 125–134.
Rossato L, Laine´ P, Ourry A. 2001. Nitrogen storage and remobilisation in
Brassica napus L. during the growth cycle: nitrogen fluxes within the
plant and changes in soluble protein patterns. Journal of Experimental
Botany 52: 1655–1663.
Sanetra CM, Ito O, Virmani SM, Vlek PLG. 1998. Remobilisation of
nitrogen from senescing leaves of pigeonpea (Cajanus cajan (L.)
Milsp.): genotypic differences across maturity groups? Journal of
Experimental Botany 49: 853–862.
Schjoerring JK, Bock JGH, Gammelvind L, Jensen CR, Mogensen VO.
1995. Nitrogen incorporation and remobilisation in different shoot
components of field-grown winter oilseed rape (Brassica napus L.)
as affected by rate of nitrogen application and irrigation. Plant and Soil
177: 255–264.
Smith CJ, Whitfield DM, Gyles OA, Wright GC. 1989. Nitrogen fertilizer
balance of irrigated wheat grown on red-brown earth in southeastern
Australia. Field Crops Research 21: 265–275.
Tittonel ED, Chaput JP, Letoublon F, Bonnot O. 1988. Besoins
en éléments minéraux du colza cultive´ en France. In:
Physiologie et élaboration du rendement du Colza. Paris: Cetiom
Editions, 68–72.
Triboı¨-Blondel AM. 1988. Mise en place et fonctionnement des
feuilles de colza d’hiver : relations azote-carbone et se´nescence. In:
Physiologie et élaboration du rendement du Colza. Paris: Cetiom
Editions, 111–120.
v/c Dad-
-
 2
2
-
 1
1


